Việc đóng gói thuốc là lớp bảo vệ đầu tiên và cuối cùng cho chất lượng, độ ổn định và an toàn sử dụng của thuốc. Bởi thuốc là dược phẩm, ảnh hưởng trực tiếp tới sức khỏe của người dùng nên phải có quy định chuyên ngành nhằm bảo đảm thuốc lưu hành đáp ứng các yêu cầu về chất lượng và truy xuất nguồn gốc. Vì vậy, bài viết này sẽ nêu ra khung pháp lý và những quy định áp dụng tại Việt Nam, giải thích các yêu cầu kỹ thuật theo từng dạng bào chế, làm rõ quy tắc về nhãn và tờ hướng dẫn sử dụng, và gợi ý các bước triển khai để doanh nghiệp sản xuất thực hiện đúng chuẩn.
Các khung pháp lý và tiêu chuẩn trong việc đóng bao bì thuốc tại Việt Nam
Luật Dược 2016

Luật Dược 2016 là nền tảng pháp lý chính điều chỉnh hoạt động sản xuất, lưu hành, ghi nhãn và kiểm nghiệm thuốc. Trong đó có khái niệm và yêu cầu với bao bì tiếp xúc trực tiếp với thuốc. Khi thiết kế, lựa chọn vật liệu, doanh nghiệp cần bảo đảm bao bì đáp ứng tiêu chuẩn chất lượng và tương thích với dược chất để được chấp nhận trong hồ sơ đăng ký.
Ghi nhãn thuốc và tờ hướng dẫn sử dụng

Thông tư 01/2018/TT-BYT quy định nội dung và cách ghi nhãn thuốc, nguyên liệu làm thuốc, cùng yêu cầu về tờ hướng dẫn sử dụng bằng tiếng Việt đi kèm mỗi đơn vị bao bì thương phẩm. Quy định này giúp thống nhất thông tin tối thiểu cần có, từ tên thuốc, hoạt chất, hàm lượng đến hạn dùng, số lô và hướng dẫn bảo quản, bảo đảm người bệnh và nhân viên y tế tra cứu chính xác.
Từ ngày 15/01/2024, Thông tư 23/2023/TT-BYT có hiệu lực, sửa đổi một số nội dung của Thông tư 01, trong đó có cơ chế cập nhật, bổ sung nhãn và tờ hướng dẫn sử dụng trong những tình huống nhất định. Việc nắm rõ điểm sửa đổi giúp doanh nghiệp tránh sai sót khi hoàn thiện hồ sơ lưu hành và khi đưa thuốc ra thị trường.
Thực hành tốt sản xuất thuốc (GMP)
Đóng gói thuốc là một công đoạn trong hệ thống GMP, vì vậy quy trình, thiết bị và nhân sự phải đáp ứng nguyên tắc, tiêu chuẩn GMP mà Bộ Y tế công bố và cập nhật, bao gồm cả hướng dẫn về bố trí khu vực, vệ sinh và kiểm soát nhiễm chéo. Với một số nhóm thuốc nguy cơ cao, yêu cầu về dây chuyền, khu vực và kiểm soát càng nghiêm ngặt hơn để bảo đảm an toàn cho sản phẩm và môi trường sản xuất.
Yêu cầu kỹ thuật theo dạng bào chế & kiểu bao bì
Thuốc viên và thuốc nang đóng vỉ, lọ thủy tinh hoặc nhựa
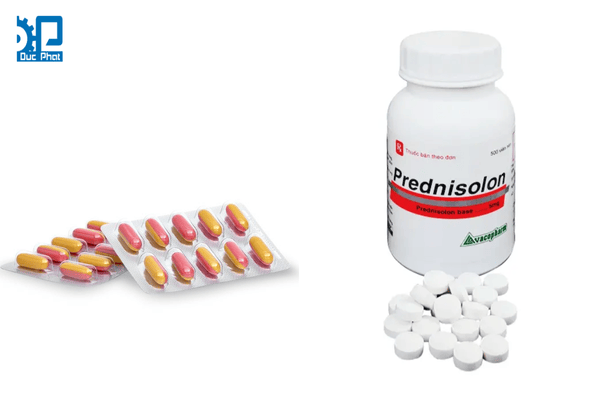
Với viên nén và viên nang, thách thức lớn nhất thường đến từ độ ẩm và ánh sáng vì chúng có thể làm viên hút ẩm, mềm hoặc phân hủy hoạt chất nhanh hơn dự kiến. Bao bì vỉ giúp chia liều rõ ràng, giảm mở nắp nhiều lần, còn lọ HDPE, PET hoặc thủy tinh thuận tiện cho đóng gói số lượng lớn; mỗi lựa chọn có mức độ bảo vệ ẩm khác nhau, do đó cần cân nhắc kết hợp với màng phủ chống ẩm hoặc lớp cản quang khi công thức nhạy sáng.
Khả năng dễ mở và dễ tách liều cũng quan trọng vì người dùng cần dùng đúng liều, đúng thời điểm mà không làm hỏng các đơn vị còn lại. Doanh nghiệp nên thử nghiệm thực tế về độ kín nắp, lực mở nắp và độ nguyên vẹn mép hàn, từ đó điều chỉnh vật liệu nắp, ron và quy trình siết nắp để bảo đảm an toàn vận chuyển và sử dụng.
Thuốc bột và thuốc hạt đóng gói, lọ nhỏ

Thuốc bột và hạt thường rất nhạy ẩm nên bao bì cần tạo hàng rào ẩm tốt và kín khí, đặc biệt trong điều kiện nhiệt đới ẩm. Vật liệu ghép nhiều lớp có thể mang lại hiệu năng chống ẩm và chống oxy, trong khi keo hàn và nhiệt hàn phải được tối ưu để đường mép không bong trong vận chuyển, nhưng vẫn xé mở dễ dàng khi sử dụng.
Khi dùng gói nhỏ, đường xé định hướng và cảnh báo cách mở nên được thể hiện rõ ràng để hạn chế rơi vãi. Với lọ, doanh nghiệp có thể cân nhắc bổ sung gói hút ẩm phù hợp và ghi rõ hướng dẫn bảo quản sau mở nắp; mọi biện pháp đi kèm phải được đánh giá tương thích với công thức để không phát sinh tạp nhiễm hoặc mùi lạ.
Thuốc nước không vô trùng
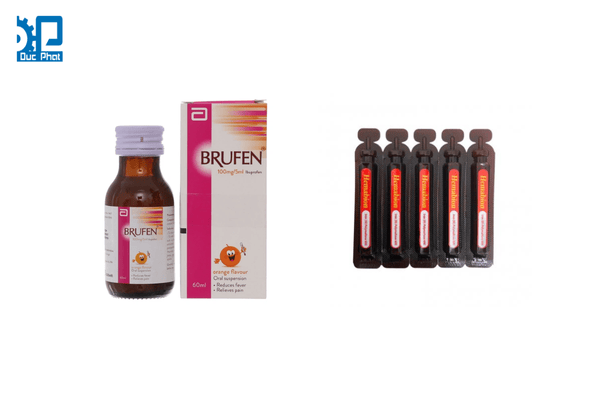
Thuốc nước không vô trùng là các loại si rô và dung dịch uống. Đối với loại thuốc nước này, mục tiêu chính là duy trì độ kín và tính toàn vẹn của nắp, đồng thời hạn chế tiếp xúc ánh sáng nếu dược chất nhạy sáng.
Thiết kế miệng rót, nút nhỏ giọt hoặc muỗng đong kèm theo giúp người dùng định liều chính xác và sạch sẽ; các chi tiết nhỏ như ren nắp, vòng co hay tem niêm cũng góp phần ngăn can thiệp trái phép. Nếu phải hạn chế tiếp xúc ánh sáng, các lọ đựng thường sẽ có màu nâu tối thay vì trong suốt.
Vật liệu tiếp xúc trực tiếp với thuốc nước cần tương thích với tá dược và dung môi, tránh hiện tượng hấp phụ hoạt chất, thôi nhiễm hay mùi vị lạ. Trước khi thương mại hóa, nhà sản xuất nên đánh giá độ kín, mô phỏng vận chuyển và thử bảo quản ở các điều kiện khắc nghiệt để xác nhận bao bì bảo vệ được sản phẩm suốt vòng đời.
Thuốc nước vô trùng

Thuốc vô trùng là các loại thuốc tiêm, dịch truyền hoặc thuốc nhỏ mắt,… Với thuốc vô trùng, yêu cầu cao nhất là vô trùng và độ kín tuyệt đối của hệ bao bì. Lọ thủy tinh, ống tiêm tiền nạp hoặc chai truyền phải được rửa, tiệt khuẩn và đóng kín trong điều kiện kiểm soát chặt chẽ; mọi sai số ở nắp cao su, nút kín hay cổ lọ đều có thể dẫn tới mất vô trùng hoặc giảm hạn dùng.
Doanh nghiệp cần kiểm tra độ kín sau đóng gói bằng các phương pháp thích hợp, đồng thời triển khai chiến lược kiểm soát nhiễm trong toàn bộ dây chuyền. Bao bì vô trùng cũng phải chịu được quy trình tiệt khuẩn được chọn, ví dụ hấp ướt hay chiếu xạ, nên việc lựa chọn vật liệu nắp, lớp lót và gioăng cần được thẩm định sớm từ giai đoạn phát triển.
Yêu cầu về nhãn, tờ hướng dẫn sử dụng & bao bì thứ cấp
Nội dung bắt buộc trên nhãn
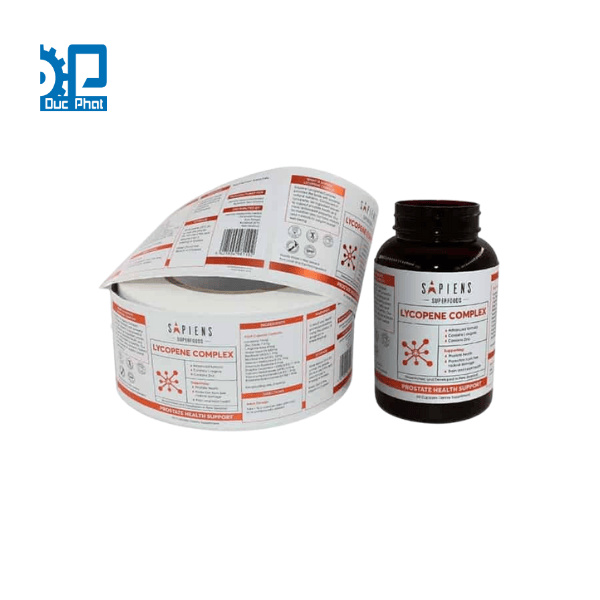
Nhãn thuốc phải thể hiện đầy đủ các thông tin cốt lõi, bao gồm tên thuốc, hoạt chất, dạng bào chế, hàm lượng, quy cách đóng gói, số đăng ký, số lô, hạn dùng, điều kiện bảo quản, tên và địa chỉ cơ sở sản xuất cũng như cơ sở đăng ký. Những thông tin này cần được trình bày rõ ràng, nhất quán với hồ sơ đăng ký đã được phê duyệt, và sử dụng tiếng Việt theo quy định để mọi đối tượng dễ đọc và tra cứu.
Ở một số trường hợp, thuốc nhập khẩu có thể bổ sung nhãn phụ bằng tiếng Việt để bảo đảm khớp với nhãn được phê duyệt, và doanh nghiệp phải hoàn tất cập nhật theo thời hạn được quy định.
Tờ hướng dẫn sử dụng đi kèm

Mỗi bao bì thương phẩm phải có tờ hướng dẫn sử dụng bằng tiếng Việt, trình bày cách dùng, liều dùng, chống chỉ định, cảnh báo, tương tác và các lưu ý đặc biệt. Khi không có bao bì ngoài, doanh nghiệp cần in hoặc gắn thông tin hướng dẫn trực tiếp trên bao bì tiếp xúc với thuốc để người dùng luôn tiếp cận được thông tin an toàn. Trình bày khoa học, dễ đọc, và tránh thuật ngữ khó hiểu sẽ giúp giảm sai sót sử dụng trên thực tế.
Trong quá trình cập nhật, doanh nghiệp phải rà soát sự phù hợp giữa tờ hướng dẫn sử dụng, nhãn, và dữ liệu an toàn hiệu lực mới nhất từ hồ sơ đăng ký. Các trường hợp được phép thay thế, bổ sung tờ hướng dẫn sử dụng sau thông quan cần tuân thủ điều kiện và thủ tục mà Bộ Y tế đã sửa đổi, tránh tình trạng nhầm phiên bản gây rủi ro pháp lý và vận hành.
Bao bì thứ cấp và tính dễ đọc

Bao bì thứ cấp, như hộp giấy bên ngoài, có vai trò bảo vệ sản phẩm khỏi va đập, nắng nóng và mất mát tờ hướng dẫn. Trên bao bì thứ cấp, thông tin cần đồng bộ với bao bì sơ cấp và nhãn được phê duyệt; cách bố cục, cỡ chữ và độ tương phản nên được thiết kế sao cho dễ đọc trong điều kiện ánh sáng thường, kể cả với người cao tuổi hoặc nhân viên kho dược.
Với sản phẩm có nhiều liều hoặc nhiều dạng trình bày, quy chuẩn đặt tên quy cách và mã hóa nội bộ nên được hoạch định ngay từ đầu để giảm lỗi nhầm lẫn. Việc áp dụng mã vạch hoặc mã 2D theo chuẩn GS1 hỗ trợ quản trị kho và truy xuất, đồng thời tạo nền tảng cho số hóa dữ liệu lô sản xuất phục vụ thu hồi nhanh khi cần.
Kết luận
Đóng gói thuốc là mắt xích quan trọng trong hệ thống đảm bảo chất lượng, kết nối giữa công thức, quy trình sản xuất và trải nghiệm sử dụng của người bệnh. Khi doanh nghiệp hiểu rõ khung pháp lý Việt Nam, nắm vững yêu cầu theo từng dạng bào chế và triển khai một quy trình đóng gói có thẩm định đầy đủ, sản phẩm sẽ đi đến tay người dùng với độ an toàn và tin cậy cao.


